

近日,南京林业大学黄超伯教授、熊燃华教授联合比利时根特大学Stefaan C. De Smedt院士和Kevin Braeckmans教授在Nature Nanotechnology上在线发表了一篇题为“Photothermal nanofibers enable safe engineering of therapeutic cells”的研究型论文。该研究表明嵌入生物相容性电纺纳米纤维中的光敏氧化铁纳米颗粒通过光热效应诱导膜通透性,并且不需要与纳米颗粒直接细胞接触。光热纳米纤维已经成功地用于传递效应分子,包括CRISPR-Cas9核糖核蛋白复合物和短干扰RNA,到粘附和悬浮细胞,包括胚胎干细胞和难以转染的T细胞,而不影响细胞增殖或表型。作者表示,使用光热纳米纤维进行细胞内递送是一个有前景的概念,可以安全、更有效地用于细胞免疫治疗。

图1.研究成果设计图
主要研究内容包括:
(1)研究了光敏纳米粒嵌合的纳米纤维结构与胞内递送效率的构效关系;重点关注静电纺丝制备参数,控制嵌合光敏纳米粒与纤维表面接触的细胞距离,以保证嵌合光敏纳米粒生成的光热效应能有效增强细胞膜通透性,得到最优光响应纳米纤维结构,用于生物大分子药物胞内递送;
(2)进一步,研究了光响应纳米粒生成的光热效应与细胞膜作用机理;主要关注光辐照光敏纳米粒生成光热效应的过程,及其作用于细胞膜增强细胞膜渗透性的机制;
(3)应用小鼠模型,采用最优光响应纳米纤维递送生物高分子药物小干扰核酸到人体免疫T细胞内,以形抑制PD-1蛋白的表达,从而提供治疗T细胞(CAR-T细胞)抑制肿瘤增长,最终达到增强治疗效果的目的。
1、光热纳米纤维的制备与表征
将聚己内酯 (PCL) 和 氧化铁纳米粒(IONPs) 以不同重量百分比溶解在 N,N-二甲基甲酰胺 (DMF)-四氢呋喃 (THF) 中制成混合物,然后进行静电纺丝制备成光热纳米纤维。
从SEM图和TEM图可以看出,纤维的平均直径约为 300 nm,直径不随 IONP 浓度变化而变化(图 2b-d)。共聚焦显微镜显示,静电纺丝 1 小时后,光热纳米纤维(PEN )网的厚度逐渐增加至 4 μm(图 2e、f)。当向纳米纤维中添加越来越多的 IONP 时,PEN 网的厚度没有显着变化(图2g)。
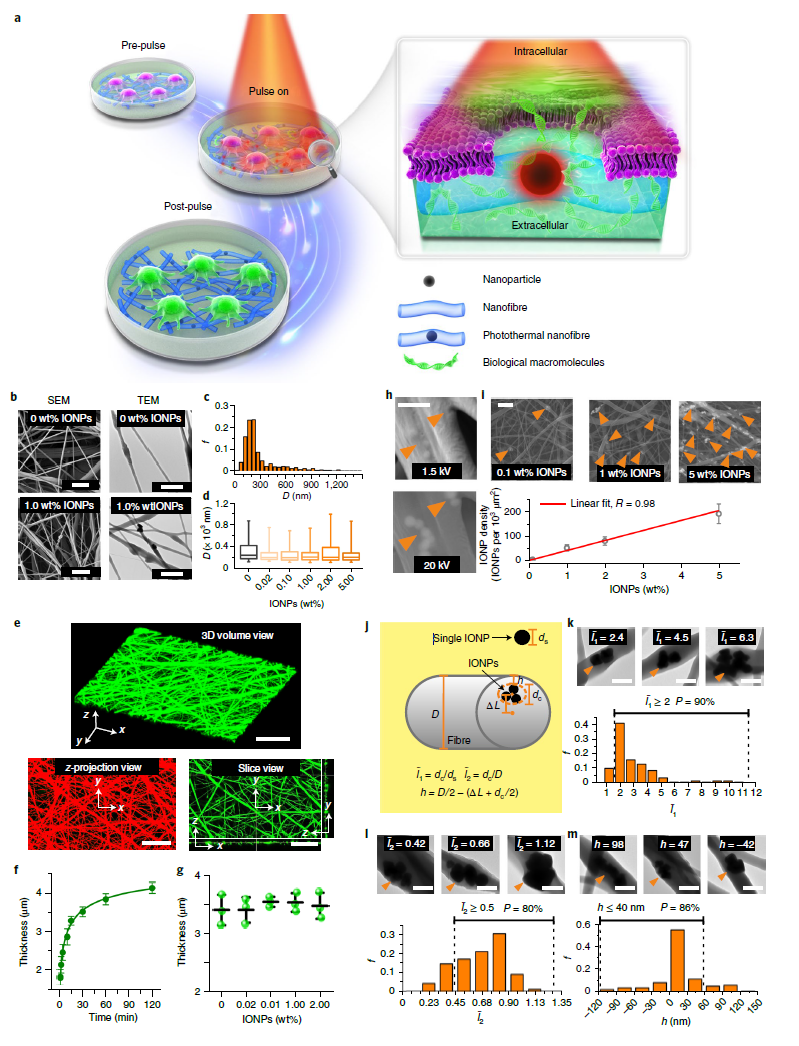
图2:光热纳米纤维胞内递送概念及光热纳米纤维的表征。(a)光热纳米纤维的胞内递送原理示意图。(b)含有0和1 wt%光响应纳米粒的纳米纤维的SEM和TEM图像。(c)不含纳米粒的纳米纤维直径分布图。(d)含不同纳米粒(0 - 5%)的纳米纤维直径。(e)纳米纤维(不含纳米粒)的共聚焦显微镜图像。(f)纤维膜厚度随着静电纺丝时间的变化。(g)30 min纺丝后,纳米纤维膜厚度与含纳米粒的关系。(h)20 kV的SEM成像清楚地显示了纳米粒在纤维内部(下),而在1.5 kV较低电压下则不是这样。(i)单位面积的纳米粒团簇与纳米粒含量的关系。(j-m)纳米粒在纳米纤维中的分布示意图以及相应结果。
2. 光热纳米纤维高效、安全的大分子胞内传递
首先,光热纳米纤维被证明能高效、安全递送大分子到HeLa贴壁细胞。通过共聚焦显微镜图像结果定量分析,得到增加激光能量密度或纳米粒的含量能提高递送效率,但细胞毒性也逐渐增加;发现当激光能量密度为0.08 J/cm2 和纳米粒含量为1%时,得到最优胞内递送结果(图3a)。接下来,测试了光热纳米纤维对Jurkat悬浮细胞的递送效率。发现当激光能量密度为0.16 J/cm2和纳米粒含量为2%时,得到最优胞内递送结果(图3b)。最后,质谱检测结果表明包裹在纳米纤维中的纳米粒没有泄露到溶液或细胞(图3c-f)。
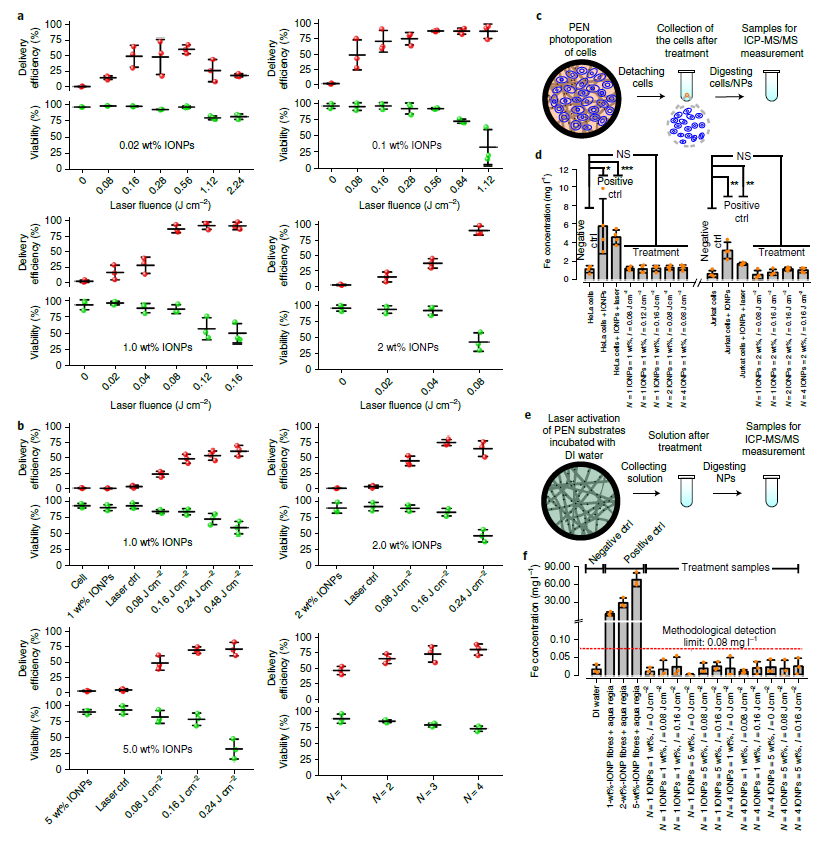
图3:光热纳米纤维高效、安全的大分子胞内传递。(a)红色荧光标记的10 kDa葡聚糖(RD10)的HeLa贴壁细胞递送效率、存活率与激光能量密度、光敏纳米粒含量的关系。(b)Jurkat悬浮细胞递送效率、存活率与激光能量密度、光敏纳米粒含量的关系。(c-d)光照射后ICP-MS/MS测定细胞中Fe含量的实验示意图;不同实验条件下,Fe含量的测量结果。(e-f)光照射后ICP-MS/MS测定水溶液中Fe含量的实验步骤示意图,以及不同实验条件下的Fe含量的测量结果。
3. 光热纳米纤维应用于生物大分子siRNA或CRISPR/Cas9的胞内递送研究
成功实现模型大分子胞内递送后,光热纳米纤维进一步被应用于生物功能大分子siRNA或CRISPR/Cas9的胞内递送。首先,光热纳米纤维将抗绿色荧光蛋白(GFP)的siRNA递送到稳定表达GFP的H1299细胞中。研究结果表明随着siRNA浓度(0.5, 1, 2和5µM)的增加,GFP的静默效率越高,同时不影响细胞活性(图4a-f)。接着,光热纳米纤维将敲除GFP表达的RNPs递送到H1299细胞中。研究结果表明GFP的敲除效率随着RNP浓度的增加而增加,最高RNP浓度的GFP敲除效率可达80%(图4g-j)。
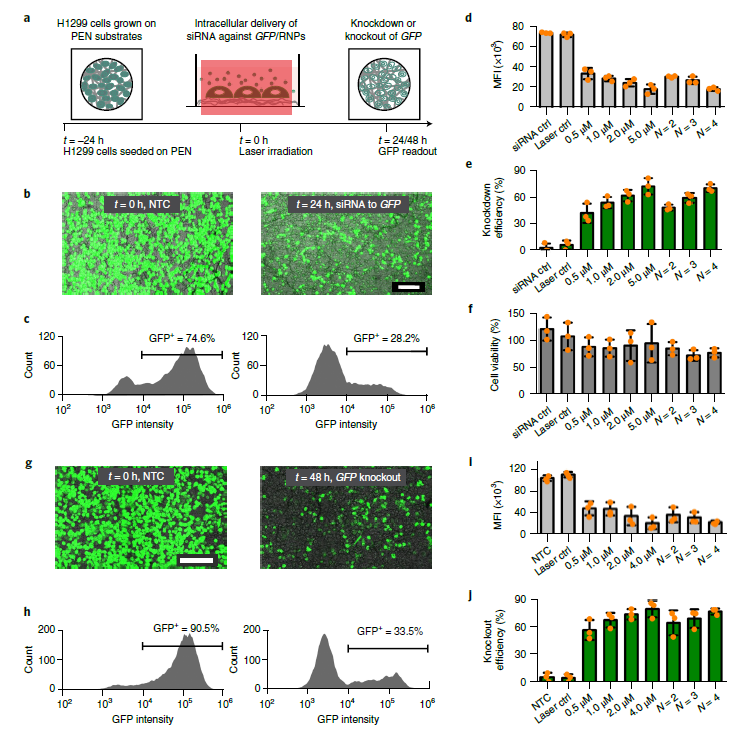
图4:光热纳米纤维应用于生物大分子siRNA或CRISPR/Cas9RNPs的胞内递送研究。(a)光热纳米纤维将siRNA或RNPs递送到H1299细胞以抑制或敲除绿色荧光蛋白(GFP)表达的实验示意图。(b)共聚焦显微镜图像显示了对照和siRNA胞内递送的H1299细胞GFP的表达。(c)相应的流式细胞仪直方图结果。(d-f)24小时后H1299细胞在不同情况下的GFP表达和活性结果。(g-h)光热纳米纤维将RNPs递送到H1299细胞以敲除GFP表达;共聚焦显微镜图像和相应的流式细胞仪结果。(i-j)48小时后H1299细胞在不同情况下的GFP敲除和活性结果。
4. 光热纳米纤维应用于人胚胎干细胞(hESC)高效安全的生物大分子胞内递送
在该工作中,光热纳米纤维还被应用于细胞治疗相关的人胚胎干细胞(hESCs)的胞内递送。实验结果表明随着递送效率逐渐提高,但同时细胞活性也降低了;当I=0.08 J/cm2时,获得最优递送效率为63%;与此相比,传统电穿孔方法在最优程序(CE-118)的递送率仅为25%(图5a-d)。同时,研究结果表明光热纳米纤维处理后的人胚胎干细胞不影响干细胞功能特性(图5e-i)。最后,光热纳米纤维成功的应用到递送RNPs到hESCs细胞,以敲除X染色体上的IL-2Rgamma (IL-2R)基因表达(图5j-k)。
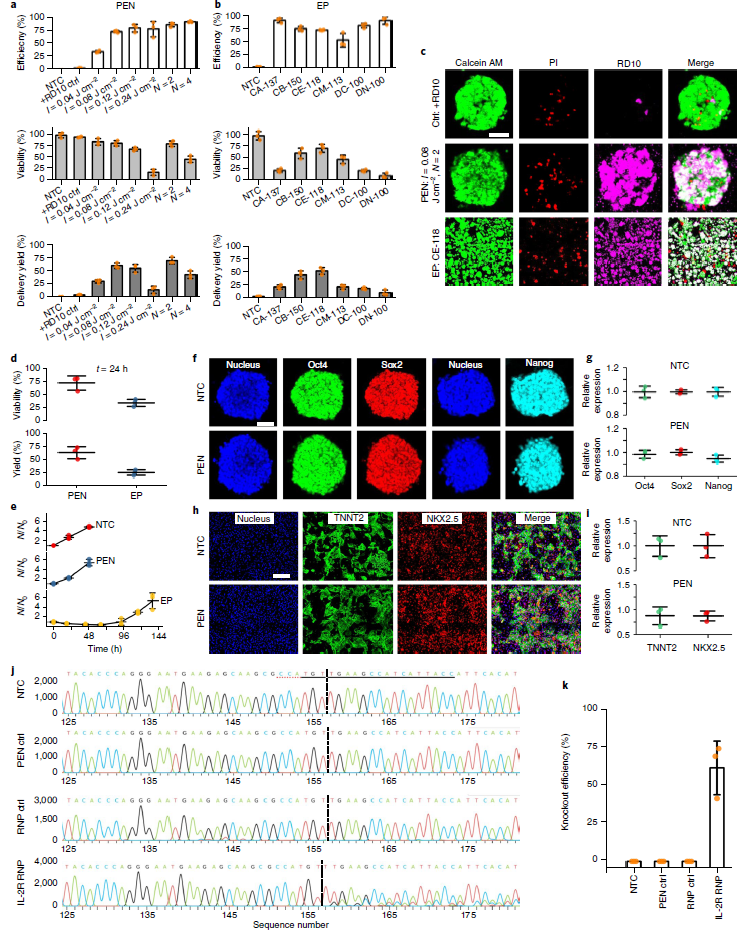
图5:光热纳米纤维应用于人胚胎干细胞(hESC)高效安全的生物大分子胞内递送。(a)不同实验条件下,hESC胞内递送效率和细胞活性。(b)不同电穿孔条件下的hESC递送效率和细胞活性。(c)共聚焦显微镜图像显示了hESC递送效率和细胞活性。(d)在最优光热纳米纤维和电穿孔实验条件下处理hESC后,24 h后两者细胞存活率和递送效率。(e)最优实验条件下处理hESC后,细胞生长效率。(f)光热纳米纤维处理hESCs24小时后,转录因子Oct4 (Pou5f1)、Sox2和Nanog免疫染色共聚焦显微镜图像。(g)Oct4 (Pou5f1)、Sox2和Nanog转录因子的量化结果。(h)标记特异蛋白TNNT2和NKX2.5的免疫染色共聚焦图像展示了hESCs分化为心肌细胞。(i)心肌细胞TNNT2和NKX2.5的量化结果。(j)hESCs在不同实验情况下的Sanger基因序列。(k)通过Sanger测序分析了IL-2R敲除效率。
5. 光热纳米纤维应用于人T细胞高效安全的生物大分子胞内递送
最后,光热纳米纤维被应用于人供体来源的T细胞的胞内递送。研究发现光热纳米纤维的最佳递送效率为40.7%,而传统电穿孔方法为19.3%,尽管在递送siRNA以抗PD-1蛋白表达效率类似(图6a-d)。为保证递送安全性,递送方法应该最小限度地干扰治疗细胞的功能特性。结果表明光热纳米纤维对T细胞形态、表型、激活状态的功能没有显著影响,而以此相反的是电穿孔对T细胞功能影响较大(图6e-f)。最终导致了电穿孔处理的T细胞在目标细胞杀伤功能减弱,而光热纳米纤维处理的T细胞能保持原有功能特性(图6i-j,图7)。
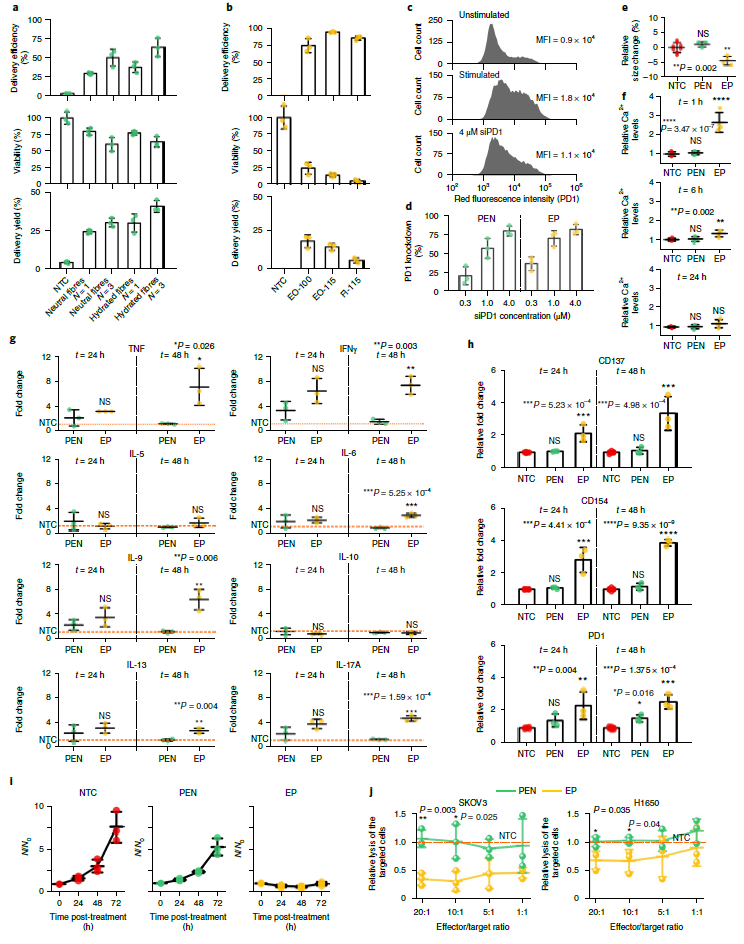
图6:光热纳米纤维应用于人T细胞高效安全的生物大分子胞内递送。(a)光热纳米纤维应用于T细胞递送。(b)电穿孔后的T细胞递送。(c-d)光热纳米纤维和电穿孔方法递送小干扰核酸siPD1到T细胞以抑制PD1蛋白表达。(e)光热纳米纤维和电穿孔方法处理T细胞1小时后,对细胞尺寸的影响。(f)光热纳米纤维和电穿孔方法处理T细胞后,相对钙离子随时间的变化。(g)光热纳米纤维和电穿孔方法处理T细胞后,几种关键促炎或抗炎细胞因子的分泌情况。(h)光热纳米纤维和电穿孔方法处理T细胞后,激活标记物CD137、CD154以及PD1的蛋白表达情况。(i)光热纳米纤维和电穿孔方法处理T细胞后,细胞的增殖情况。(j)光热纳米纤维和电穿孔方法处理T细胞后,细胞在体外对目标细胞杀伤情况。
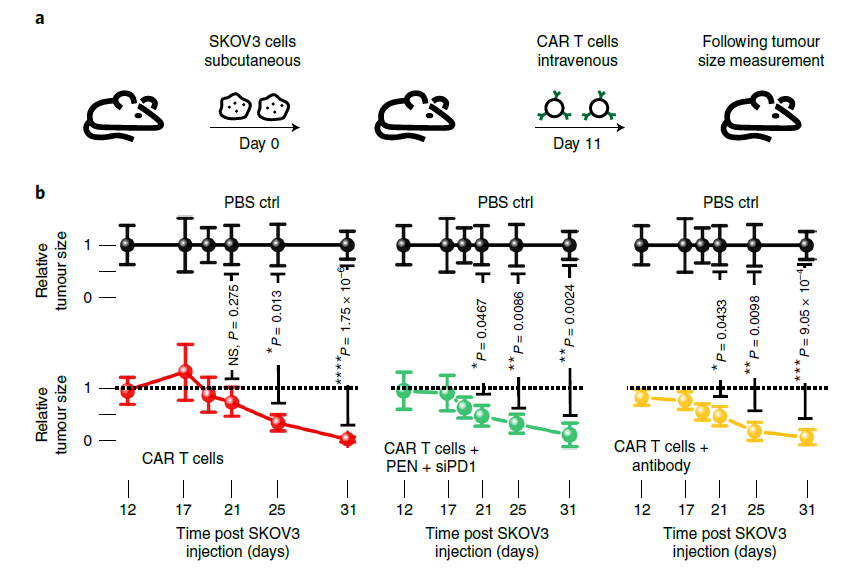
图7:光热纳米纤维处理后的T细胞在体内保持着细胞功能特性。(a)光热纳米纤维将siRNA递送到CAR-T细胞以证明在SKOV3肿瘤小鼠模型有效性的实验示意图。(b)静脉注射CAR-T细胞(阴性对照,n=5)、光热纳米纤维将siPD1递送到CAR-T细胞(实验组,n=4)、CAR-T细胞联合PD1-抗体给药(阳性对照,n=4)的肿瘤大小随时间变化。
总之,该工作开发了一种新型的生物大分子胞内递送方法,其不仅保持了光敏纳米粒在光响应胞内递送的主要优点,同时避免了其致命缺点,即光敏纳米粒残留在细胞内产生潜在的毒副作用。通过优化光敏纳米粒在纳米纤维的嵌合度,以控制作用于细胞的光热效应,创造性地将光响应纳米粒胞内递送与静电纺丝技术相结合,实现了纳米粒与细胞非接触的生物大分子药物安全高效的胞内递送,增强生物大分子药物药效,有望进一步提高疾病治疗效果。
论文链接:
https://www.nature.com/articles/s41565-021-00976-3
实验室主页:
https://www.x-mol.com/groups/nfu-ugent
