
组织工程支架作为一种人工细胞外基质,可促进组织再生和修复。因此,支架的内部结构对细胞粘附、生长和迁移至关重要。在本文中,基于超临界二氧化碳发泡技术,通过引入第二相聚乳酸静电纺丝纳米纤维,制备了一种由非均相纳米纤维诱导的新型三维(3D)多孔聚己内酯/聚乳酸组织工程支架。扫描电镜结果表明,所制备的支架具有明显的纳米纤维结构和3D网状多孔结构。此外,还系统地探讨了发泡温度对孔隙形态的影响。拉伸试验和水接触角测量表明,新型支架具有良好的机械性能和亲水性。横断面人脐带内皮细胞(HUVEC)培养结果表明,该支架具有较好的生物相容性,能显著促进HUVECs的粘附、迁移和通透性。单细胞迁移试验表明3D多孔支架有效促进了HUVEC迁移。因此,3D多孔支架在血管补片领域具有巨大的应用潜力。
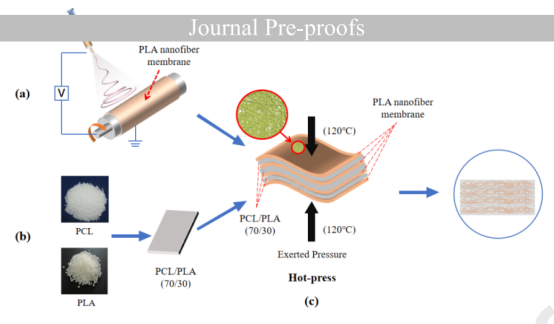
图1.多层PCL/PLA复合膜的制备示意图。
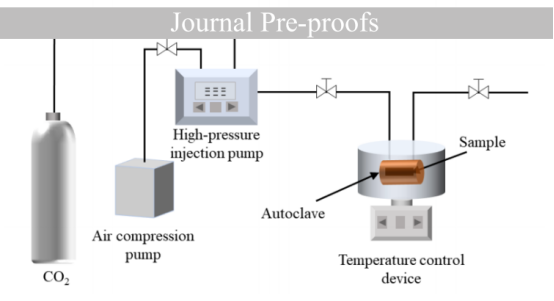
图2.间歇微孔发泡工艺示意图。

图3.(a)不同支架的照片,(b-c)PLA纤维的SEM图像和纤维直径分布,(d)多层PCL/PLA复合膜的表面形貌,以及(e)多层PCL/PLA复合膜的横截面形貌。

图4.不同样品形貌的SEM图像:(a)发泡PCL/PLA(70/30)膜,(b)未发泡多层PCL/PLA复合膜,(c-d)发泡多层PCL/PLA复合膜。
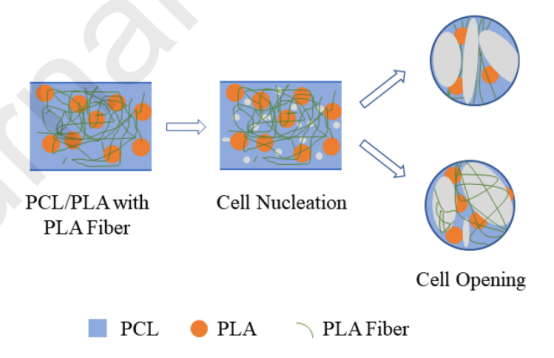
图5.网状孔隙结构形成示意图。
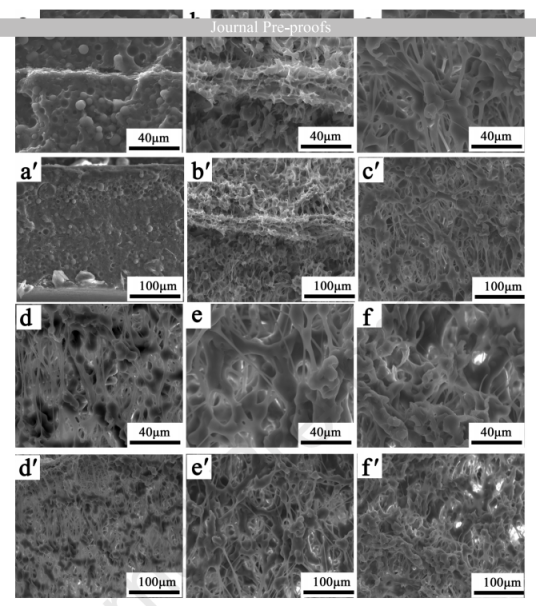
图6.复合膜的横截面以及不同温度发泡的复合材料的形貌:(a)和(a')未发泡,(b)和(b')45℃,(c)和(c')50℃,(d)和(d')55℃,(e)和(e')60℃,(f)和(f')65℃。
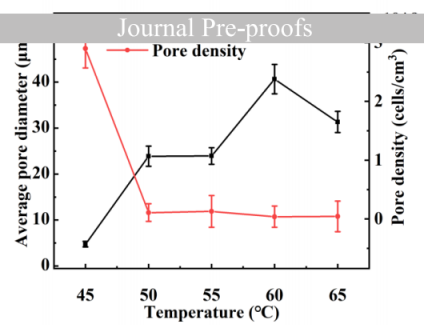
图7.发泡温度对微孔发泡多层PCL/PLA复合膜孔径和密度的影响。
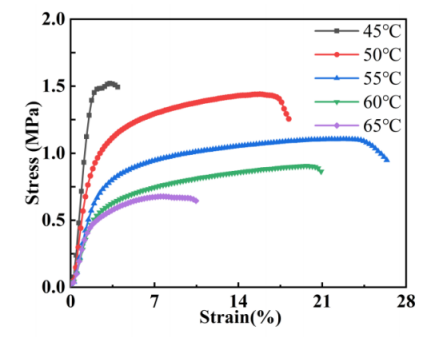
图8.不同温度发泡的多层PCL/PLA复合膜的应力-应变曲线。
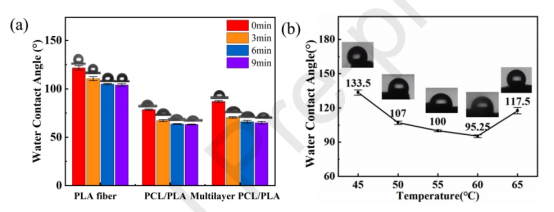
图9.(a)PLA纤维对PCL/PLA(70/30)薄膜WCA的影响;(b)不同温度发泡的多层PCL/PLA复合膜的WCA(*:p<0.5)。
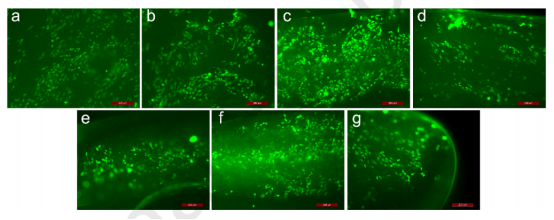
图10.不同样品的细胞活性:(a)PLA纤维;(b)发泡的PCL/PLA(70/30)薄膜;(c-g)不同温度下发泡的多层PCL/PLA复合膜,包括45℃、50℃、55℃、60℃和65℃。
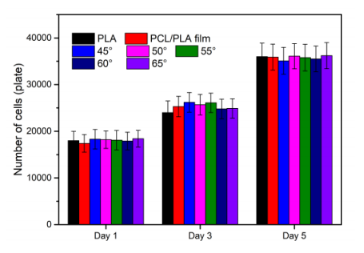
图11.第1、3和5天不同样品中的CCK-8细胞增殖:PLA纤维、发泡PCL/PLA(70/30)薄膜和发泡多层PCL/PLA复合材料。
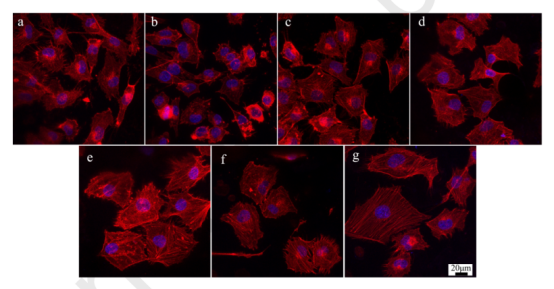
图12.不同样品的HUVEC形态:(a)PLA纤维;(b)发泡PCL/PLA(70/30)薄膜;(c-g)不同温度发泡的多层PCL/PLA复合膜,包括45℃、50℃、55℃、60℃和65℃。

图13.HUVEC在不同样品上的粘附和迁移:(a)PLA纤维;(b)发泡PCL/PLA(70/30)薄膜;(c-g)不同温度发泡的多层PCL/PLA复合膜,包括45℃、50℃、55℃、60℃和65℃。
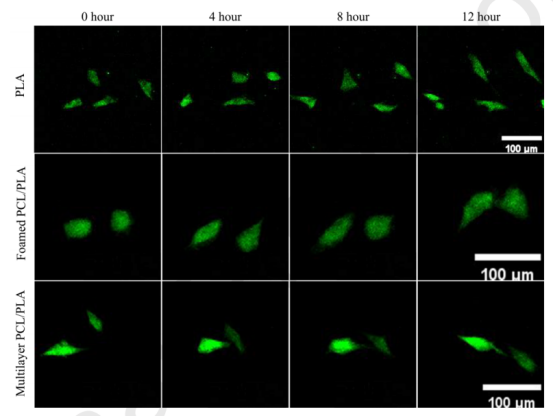
图14.HUVEC在不同样品上的迁移:(a)PLA纤维;(b)发泡PCL/PLA(70/30)薄膜;(c)发泡多层PCL/PLA复合膜。
