
DOI:10.1016/j.eurpolymj.2020.109675
目前聚合物敷料有望具有多重功能。敷料除了作为物理屏障外,还可以为受伤的组织物种提供更快和无痛的伤口愈合过程。用这种方法,可以设计出旨在使药物释放的敷料。调节药物释放动力学的可能性是为了使药物释放系统适应于特定的治疗而需要实现的特性。然而,亲水性药物和疏水性聚合物的不相容性阻碍了这种调节,并且不能有效地实现长期释放。在此,研究者介绍了聚乳酸(PLA)膜的设计,该膜包含能够存储亲水性阴离子药物(源自非甾体类抗炎性萘普生)的铁基层状双氢氧化物(LDH)颗粒。LDH颗粒是组成多功能复合材料的理想候选材料。它们可以呈现出多种生物相容性组合物,具有较高的包封能力,并且除了协助组织再生过程外,还倾向于促进药物自身的持续释放。纳米纤维膜是通过将电纺PLA和电喷雾LDH组合为交替层(方法A)以及同时进行两种工艺(方法B)制备的。在方法A中,通过改变PLA纤维层的厚度,可以容易地调节药物释放速率。对于包含最薄、中间和较厚的PLA层的膜,分别在1、4和17天后释放一半的药物含量,对于通过方法B制备的膜则在56小时后释放一半的药物含量。对于最薄的膜,萘普生的释放保持18天,通过方法B制备的膜为59天,对于较厚的膜为66天。这项工作可以借助通用的静电纺丝和电喷雾技术来激发具有可调药物释放特性的新型功能性膜的开发。
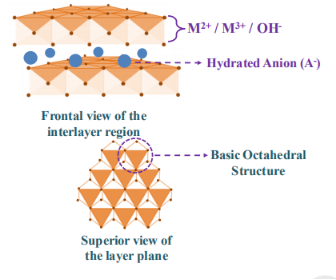
图1.LDH结构的示意图。
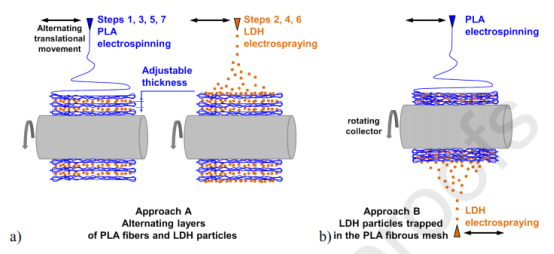
图2.在以下情况下制备复合膜:a)用于制备具有可变和可调节厚度的PLA纤维层的方法A,以及b)用于同时PLA静电纺丝和LDH电喷涂的方法B。

图3.原始的PLA膜和含有嵌入Cl-和NAP阴离子的Mg4FeAl LDHs的PLA膜的SEM显微照片,通过将4个具有不同PLA厚度(Athin-每层的静电纺丝进行15分钟,Amed-22分钟和Athick-30分钟)的电纺PLA层与3个电沉积LDH层(方法A)交替,以及同时进行静电纺丝和电喷涂(方法B)。使用BSE检测器,5 kV和10 mm左右的工作距离对样品进行分析。
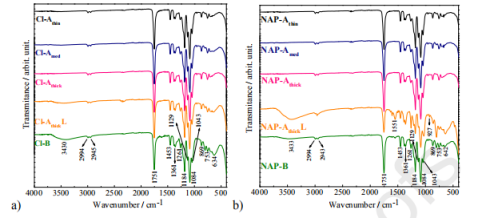
图4.含有a)Cl-LDHs颗粒和b)NAP-LDH颗粒的膜的FT-IR光谱。
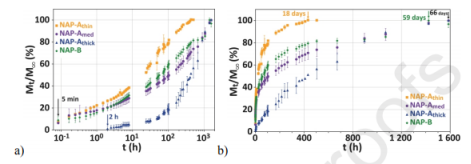
图5.药物释放曲线:萘普生的释放百分比随时间的变化。a)半对数刻度。 b)线性刻度。
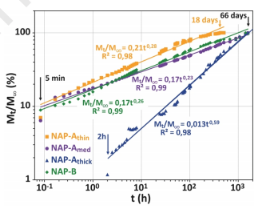
图6. Naproxen释放百分比的实验点和Ritger-Peppas模型(实线)随对数刻度中不同复合材料时间的变化。
