
DOI:10.1016/j.colsurfb.2020.111005
纤维或水凝胶形式的局部药物递送系统(LDDS)已经成为有效治疗癌症的替代方法,但由于其唯一的治疗功能而导致的有限疗效阻碍了其临床应用。在本文中,设计并合成了可微创植入的多功能LDDS,用于现场化学-光热协同治疗。在该系统中,将负载阿霉素(DOX)的聚多巴胺(PDA)纳米颗粒组装在电纺PCL-明胶(PG)纤维(PG@PDA-DOX)的表面。PG@PDA-DOX复合纳米纤维可以有效地将近红外光转化为热量,并具有出色的光稳定性。此外,低pH和近红外辐射使DOX释放明显加快。PG@PDA-DOX纤维的体外研究表明,在808nm近红外光照射下,该纤维通过诱导细胞凋亡和抑制细胞增殖,显示出有效的抗癌作用。通过微创外科手术将PG@PDA-DOX纳米纤维植入患者源性异种移植(PDX)模型的体内研究表明,复合纤维可以通过化学-光热联合作用有效地抑制肿瘤的生长,而无明显的系统性副作用。因此,该研究证明了纤维网状的微创平台在肝癌的临床治疗中具有较高的治疗功效和巨大的潜力。
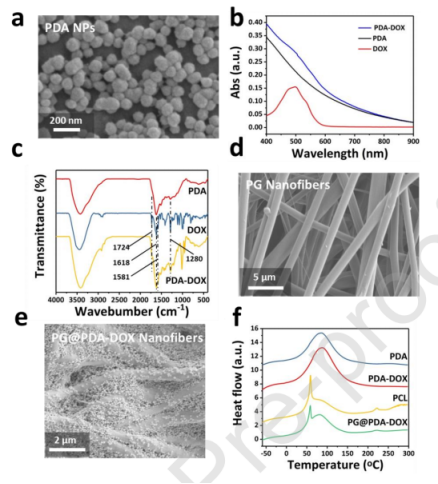
图1.(a)PDA纳米颗粒的SEM图像。(b)DOX、PDA和PDA-DOX纳米粒子的UV-Vis光谱和(c)FTIR光谱。(d)PG和(e)PG@PDA-DOX纳米纤维的SEM图像。(f)PDA、PDA-DOX、PCL和PG@PDA-DOX样品的DSC测定。
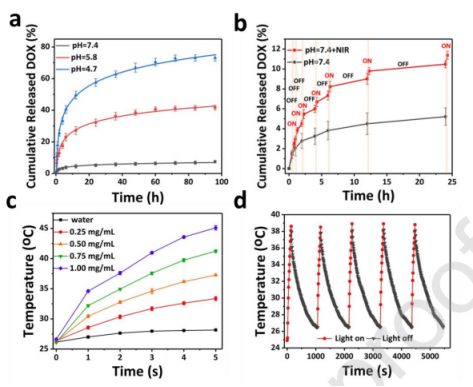
图2.在有或没有808nm 近红外照射(1.0 W cm-2)下,PG@PDA-DOX(a)在pH值变化的溶液中和(b)PBS中的累积DOX释放曲线;(c)在808nm近红外照射(1.0 W cm-2)下,不同浓度的水和PG@PDA-DOX溶液的温度变化。(d)PG@PDA-DOX水溶液(1 mg/mL)在808nm 近红外循环照射(1.0 W cm-2,120s,5个循环)下的温度变化。
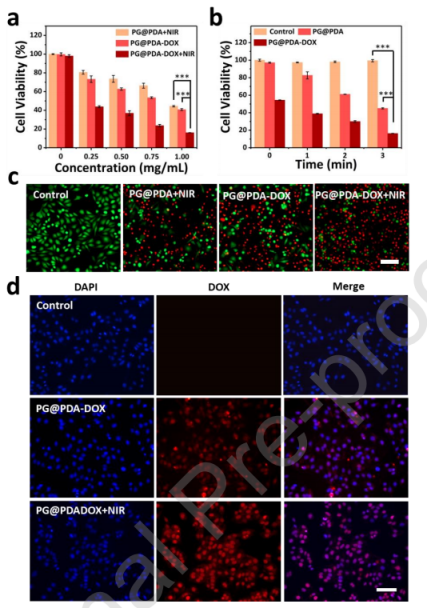
图3.(a)CCLP1细胞与808nm近红外照射(1.0 W cm-2,5分钟)后的PG@PDA、PG@PDA-DOX以及在无辐射下不同浓度的PG@PDA-DOX共孵育24小时的细胞活力。(b)CCLP1细胞与808nm近红外辐射(1.0 W cm-2,0-3分钟)下的空白对照、PG@PDA、PG@PDA-DOX共孵育24小时的细胞活力。(c)钙黄绿素AM和PI对经不同处理的CCLP1细胞共染色的荧光图像。(比例尺:100μm)(d)用辐射(808nm近红外,1.0 W cm-2)下的空白对照、PG@PDA-DOX、PG@PDA-DOX处理的CCLP1细胞的DAPI染色的荧光图像(比例尺:100μm)。
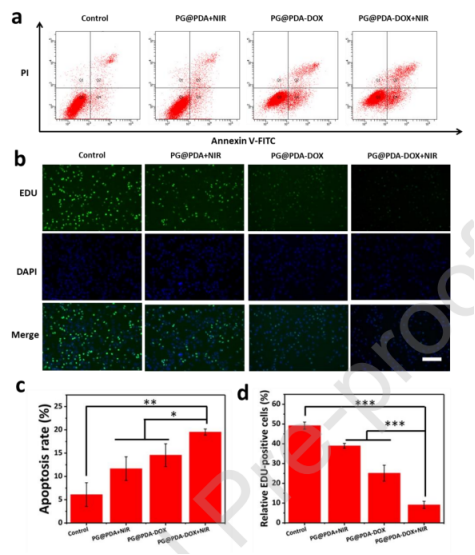
图4.(a)流式细胞术检测经不同处理的CCLP1细胞24小时的PI/膜联蛋白V凋亡。(b)经指定处理后,EDU和DAPI共染色CCLP1细胞24小时的荧光图像。(比例尺:100μm)(c)通过流式细胞术定量经不同处理的CCLP1细胞的凋亡率。(d)通过荧光图像定量经不同处理的CCLP1细胞的相对EDU阳性率。
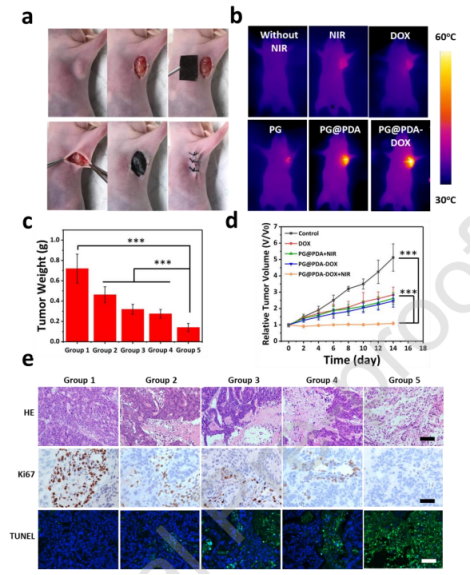
图5.(a)PDX中复合纤维网的微创手术过程。(b)照射后(808nm 近红外,1.0 W cm-2、5分钟)经不同处理的实时红外热图。(c)在第14天从不同组的小鼠收集的肿瘤重量。(d)在14天的治疗期间内,经不同治疗的小鼠的肿瘤体积增长。(e)在接受不同治疗后2天收集的肿瘤切片的H&E染色、Ki67染色和TUNEL荧光图像。(比例尺:100μm)
